- 产品描述
今年2月1日,美国食品药品(FDA)医疗器械与放射健康中心(CDRH)生物制品评估与研究中心发布了《基于安全性和基本性能的途径》指南文件。该指南旨在描述一个基于安全性和基本性能的可选途径,使510(k)提交者只需验证新器械符合FDA既定性能标准,就可以证明新器械具有与合法上市器械相当的安全性和有效性。对该指南文件进行研究探讨,有助于我们借鉴****经验和工作方式,提高我国医疗器械的审评效率,缩短审评时间,从而较好地促进我国医疗器械行业发展。
为了确定实质等同性,美国《联邦食品、药品和化妆品法案》*513(i)(1)(A)节规定,判定新器械具有与同品种医疗器械相同的预期用途,应符合如下要求:与同品种器械的技术特征相同;具有不同技术特征,与同品种器械具有实质等同性的资料,包含适当证明文件、经过认定的临床或科学数据,用于证明新器械具有与合法上市器械相当的安全性和有效性;与同品种器械相比,不会产生不同的安全性和有效性问题。
通过性能标准判定实质等同性
《基于安全性和基本性能的途径》指南(以下简称“指南文件”)的政策是扩展FDA长期以来通过简化510(k)程序应用进行医疗器械审批的方法。指南文件重点关注实质等同性分析的决**,要求510(k)提交者证明尽管存在技术差异,但新器械具有与合法上市器械相当的安全性和有效性。如果新器械满足合法上市器械在安全性和有效性方面相同特征的性能水平,FDA可以认定新器械具有与合法上市器械相当的安全性和有效性,同时支持基于表明新器械满足相应同品种器械性能水平的数据来核实实质等同性结果,而不是评审两种器械之间的直接测试数据对比。
根据指南文件中的方法,510(k)提交者可以仅证明新器械的性能符合既定性能标准,而这些性能标准可能描述在FDA指南、FDA认可共识标准和/或特殊控制文件中。通过证明新器械符合既定性能标准,提交者可以证明新器械具有与合法上市器械相当的安全性和有效性。
指南文件也提出,仅当FDA确定新器械符合以下情况时,方可使用既定性能标准:新器械适应证、技术特征不会产生与同品种器械不同的安全性和有效性问题;既定性能标准与新器械相同类型的合法上市器械的性能一致;新器械符合所有性能标准。如果新器械不能完全凭借FDA确定的既定性能标准来证明其提交材料的实质等同性,则不适合指南文件,但是,提交者仍可使用执行依据相应同品种器械进行直接性能比较的先前既定510(k)程序,包括传统、特殊和简化510(k)程序。
针对指南文件运行的工作计划
为保证指南文件顺利运行,FDA还将做以下准备:
预期用途和技术特征
FDA计划在既定性能标准中提供有关性能标准适用器械类型的信息,包括相关产品型号、适当的预期用途和适当的适应证。FDA还打算在其网站上维护适用基于安全性和基本性能途径的器械类型列表。如果对新器械是否符合FDA确定适用器械类型存有疑问,建议从相关办公室或部门寻求有关使用性能标准的适用性反馈。
确认性能标准
FDA计划在其网站为器械类型列表附上确认每种器械类型的性能标准的指南,以及指南文件中建议的测试方法(如可行)和其他相关信息。未在指南文件确定的性能标准,不得用于本程序。FDA依靠工作人员的经验和专业知识、文献资料以及对现有器械可用数据的分析,确定性能标准和相关测试方法,以支持实质等同性结果。
FDA评审数据
采用基于安全性、基本性能途径确定实质等同性的方法概述见附表。为了通过本程序获得实质等同性结果,通过提交符合FDA认可共识标准、测试方案、数据总结和/或基础数据(视情况而定)的声明,来证明新器械符合FDA认可的性能标准。必要时,FDA可以要求提交审评基础数据,证明新器械符合其既定性能标准和测试方法。
如果提供的数据不能证明新器械符合FDA确定的性能标准,将无法通过本程序确定实质等同性。提交者仍可以使用其他510(k)程序来证明实质等同性。
修改列表
FDA计划在网站上修订如前所述的器械类型列表,纳入附加器械类型,并根据指导规程(21 CFR 10.115)修订相应的性能标准和测试方法。FDA将定期评审适用标准和指南,修订或删除列表中的条目,特别是当性能标准不完全支持实质等同性决定时。从器械类型列表中删除之前,已通过基于安全性和基本性能途径获得的器械许可,将不会受到列表更改的影响
公司从2017年年初开展临床评估业务以来,为国内近两百家医疗器械企业提供了临床评估报告编撰服务,其中包括很多国内**的大型医疗器械企业。*四版欧盟临床评估指南的发布,的确给企业带来了不小的挑战,此文对主要变化进行了梳理。
主要变化之一:临床报告较新的频率
按照新版临床报告指南的要求,对于高风险或者新设备,应每年较新;对于低风险的设备,每2-5年较新。对于如何确定较新的额频率需要有定义。对于任何风险类别的器械,如果从PMS收集到的信息影响到评价或者结论,CER需要进行较新。
主要变化之二:报告编写人和评价人的
按照新版临床报告指南的要求,对于临床报告的编写人提出了要求。包括需要有相关专业的高等教育学位以及至少五年的专业经历,或者十年的专业工作经历,如果学位不够的话。如果不能满足要求,需要对其进行判定和说明。
主要变化之三:评价报告需要有明确的可测量的目标
*四版临床评估指南对于临床评估报告的目的有较明确的描述,需要与器械的安全性、性能以及风险-收益平衡进行较加清晰和详细的描述,在指南的*7部分和附件5中有详细的描述。
主要变化之四:确定技术发展水平
*四版临床评估指南对于设备的技术发展水平和处理方式的建立和文件化,提供了较加详细的描述。这包括确定设备的安全性和性能,以及被宣称的比对器械,行业的基准器械,或者其他的类似器械;需要包括风险和收益的分析。
主要变化之五:数据的科学性和有效性
*四版临床评估指南非常强调数据的科学性和有效性,包括从统计学考虑。这贯穿于整个指南文件规定的阶段,包括影响数据完整性的因素,数据的客观性和权重,文件搜集的方法,数据的评估和权重,数据是否阐述了符合性的分析。
主要变化之六:比对器械
*四版临床评估指南对于评估器械和比对器械的等效有了较加详细的规定,特别强调对于比对器械的数据的可获得性。需要从临床数据、技术参数、生物性能三个方面逐一比对,确保所有比对的内容不存在差异。
主要变化之七:比对器械的数据获得
*四版临床评估指南要求公告机构对于企业是否能够获得比对器械的数据进行挑战,这个被认为是法规的一个转折点,这要求制造商需要有一个被允许接触竞争对手的器械数据的协议。
主要变化之八:什么时候需要临床试验
*四版临床评估指南附件2详细描述了器械的风险以及制造商怎么决定是否具备了充分的临床证据。
主要变化之九:风险-收益
附件7提供了详细的指南,对于器械的安全性和性能表述;
附件7.2 讨论了风险和收益分析,包括对于风险和收益的量的评估,以及总体评价。交付后的数据**,以及可能会影响统计有效性行的因素等。
主要变化之十:售后监督和售后临床跟踪
*四版指南强调了临床评估、售后监督和售后临床评估的关系。附录12强调了公告机构需要确认PMCF被很好的策划了,以及依据所收到的数据来描述其满足CER。
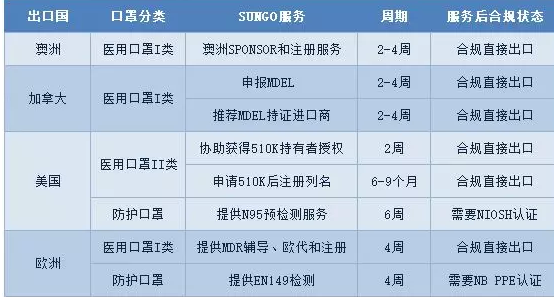
刚结束的2月后两周,我们接到很多工厂关于医用口罩产品办理国内许可证书的申请。随着国内的口罩供应逐步缓解,同时海外的疫情发展加快,口罩产品出口需求已可以清晰预见。为应对近两天广大客户关于口罩出口认证的问询,SUNGO整理相关国家和地区法规要求以及我们可以提供的服务内容。摘要见表1
表1 SUNGO提供口罩出口认证服务
Part.1
欧洲市场
欧洲市场对于口罩的管理分为两个主要类别,个人防护口罩和医用口罩。个人防护口罩主要是工业用防护,医用口罩主要是医院使用。
医用口罩
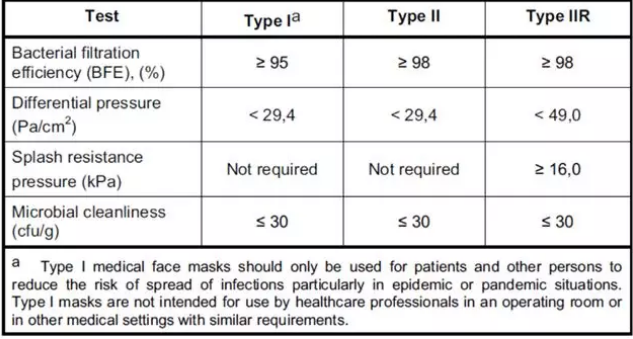
医用口罩对应的欧洲标准是EN14683,该标准对于口罩的分类如下图所示,按照BFE、呼吸阻抗和防喷溅能力分为三个类别,具体指标见表2。
SUNGO集团是**化的医疗器械法规专业技术服务商。 SUNGO品牌包括六家公司,分别是位于美国的SUNGO Technical Service Inc.,位于英国的SUNGO Certification Company Limited,位于荷兰的SUNGO Europe B.V.,位于澳洲的SUNGO Australia,位于德国的SUNGO Cert GmbH和上海沙格企业管理咨询有限公司(含上海总部、武汉分公司和广州分公司)。
欢迎来到上海沙格企业管理咨询有限公司网站,我公司位于世界上面积最大的红松原始林所在地—伊春市。 具体地址是黑龙江伊春金山屯公司街道地址,负责人是袁阳。
主要经营FDA注册和FDA510K。
你有什么需要?我们都可以帮你一一解决!我们公司主要的特色服务是:商务服务 认证服务 等,“诚信”是我们立足之本,“创新”是我们生存之源,“便捷”是我们努力的方向,用户的满意是我们最大的收益、用户的信赖是我们最大的成果。
本页链接:http://www.cg160.cn/vgy-51564874.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
关于上海沙格企业管理咨询有限公司
商铺首页 |
更多产品 |
联系方式
SUNGO集团是**化的医疗器械法规专业技术服务商。 SUNGO品牌包括六家公司,分别是位于美国的SUNGO Technical Service Inc.,位于英国的SUNGO Certification Company Limited,位于荷兰的SUNGO Europe B.V.,位于澳洲的SUNGO Australia,位于德国的SUNGO Cert GmbH和上海沙格企业管理咨询有限公司(含上海总部、武汉分公司和..
- 我要给“上海医用口罩口罩做CE认证费用 速度快”留言
- 更多产品
相关分类