- 产品描述
医用口罩ce认证EN14683检测项目和测试要求:
1、材料和结构要求
医用口罩是一种医疗器械,通常由放置,粘合或模制在织物层之间的过滤层组成。在预定使用期间,医用口罩不得分裂或撕裂。在选择过滤器和过滤层材料时,应注意清洁度(无颗粒物)。
2、设计要求
医用口罩应具有可紧密安装在佩戴者的鼻子,嘴巴和下巴上的医疗器械,并确保该面罩可紧密贴合在两侧。
医用口罩可能具有不同的形状和结构,以及其他功能,例如带有或不带有防雾功能的口罩(以保护佩戴者免受飞溅和水滴的侵害)或鼻梁(通过与鼻子保持贴合来增强贴合性)轮廓)。
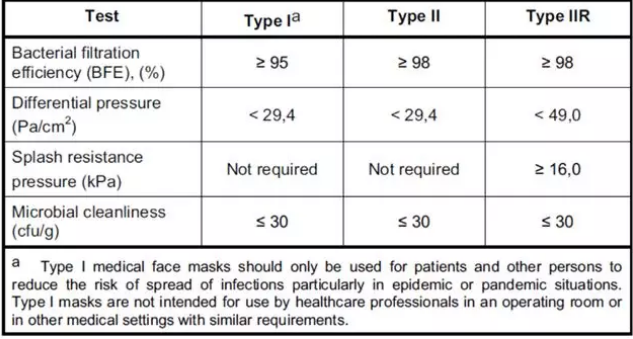
3、性能要求
通用要求:如果适用于无菌状态,则应对制成品或从制成品上切下的样品进行所有测试。
过滤效率(BFE):Type1≥95,Type2≥98
4、微生物清洁度(生物负荷)
当按照ENISO11737-1进行测试时,医用口罩的生物负荷应≤30cfu/g。
医用口罩CE认证EN14683标准测试流程:
步:客户提品图片及申请表;
第二步:环测威实验室根据提供资料进行报价;
第三步:客户确认报价后,签订立案申请表及服务协议并支付全额项目费,并准备好测试样品;
第四步:客户安排邮寄样品到实验室测试;
第五步:测试通过,报告完成、项目完成,出具CE认证证书。
CE认证,普通防护口罩,非医用的。需要做测试+CE认证,目前整个周期包含测试和出证大概在7个工作日左右。费用的话,每个机构不一样~
一般建议是做NB机构,什么是NB机构呢?可以简单理解为,被欧盟认可的机构。新手小白可以问自己的发证机构两个问题就可以判断是否靠谱了,(1)是NB机构吗?机构号可以查询?(2)证书到时候网站可查吗?
一、如果是欧洲市场出售个人防护口罩
需要满足欧盟个人防护设备标准要求,企业需选择有PPE法规授权的公告机构实施申请,需审核企业质量管理体系和CE技术文档。审核通过后可获得PPE法规的CE证书。欧盟个人防护口罩的标准是EN149,分为三类 FFP1: 过滤效果>80% ,FFP2: 过滤效果>94% ,FFP3: 过滤效果>97% 。
二、如果要在欧洲市场出售医用口罩
欧洲市场医用口罩对应的欧洲标准是EN14683,按照BFE、呼吸阻抗和防喷溅能力分为三个类别,依据产品是无菌或非无菌状态提供,其认证模式不一样。
防护口罩需要满足欧盟个人防护设备指令(PPE)的要求,防护口罩属于其中复杂设计的产品。出口欧洲需要授权的公告机构进行认证并颁发证书,认证需要的资料包括:
A)产品的型式试验报告;
B)技术文件评审
C)工厂质量体系审查。
Part.2
美国市场
美国法规对医用口罩和工业防护口罩同样是区分管理,其中医用口罩由FDA管控,而防护口罩则由NIOSH管控。大家熟知的N95口罩就来源于NIOSH对口罩分类中的一个类别。
医用口罩
美国对于医用口罩的管理机构是FDA,在FDA系统中对于口罩的分类代码有如下3个。其中一个是外科口罩,一个是口罩,一个是带有/抗病毒介质的外科口罩,见图1。
三个类别的口罩都属于规则878.4040,分类都是II类,都需要申请510K批准。那么我们正常出口美国的口罩必须的路径为:
1)进行产品测试(性能测试、生物学测试)
2)准备510K文件,提交FDA评审
3)FDA发510K批准信
4)完成工厂注册和器械列名
5)产品出口
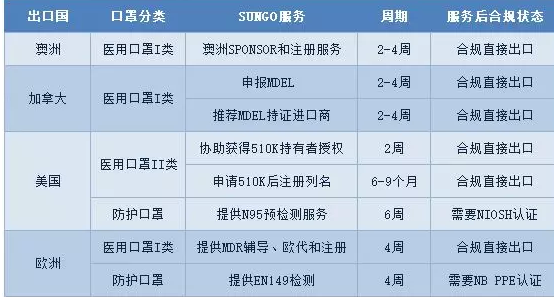
但是该过程至少需要半年以上时间。那是否有其他可选方法呢?SUNGO咨询师经过分析提供两种其他可选路径:
(1)已经获得NIOSH批准的N95口罩可以直接注册
SUNGO集团是**化的医疗器械法规专业技术服务商。 SUNGO品牌包括六家公司,分别是位于美国的SUNGO Technical Service Inc.,位于英国的SUNGO Certification Company Limited,位于荷兰的SUNGO Europe B.V.,位于澳洲的SUNGO Australia,位于德国的SUNGO Cert GmbH和上海沙格企业管理咨询有限公司(含上海总部、武汉分公司和广州分公司)。
欢迎来到上海沙格企业管理咨询有限公司网站,我公司位于世界上面积最大的红松原始林所在地—伊春市。 具体地址是黑龙江伊春金山屯公司街道地址,负责人是袁阳。
主要经营FDA注册和FDA510K。
你有什么需要?我们都可以帮你一一解决!我们公司主要的特色服务是:商务服务 认证服务 等,“诚信”是我们立足之本,“创新”是我们生存之源,“便捷”是我们努力的方向,用户的满意是我们最大的收益、用户的信赖是我们最大的成果。
本页链接:http://www.cg160.cn/vgy-51541147.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
关于上海沙格企业管理咨询有限公司
商铺首页 |
更多产品 |
联系方式
SUNGO集团是**化的医疗器械法规专业技术服务商。 SUNGO品牌包括六家公司,分别是位于美国的SUNGO Technical Service Inc.,位于英国的SUNGO Certification Company Limited,位于荷兰的SUNGO Europe B.V.,位于澳洲的SUNGO Australia,位于德国的SUNGO Cert GmbH和上海沙格企业管理咨询有限公司(含上海总部、武汉分公司和..
- 我要给“南昌口罩做CE认证和EN14683 较专业”留言
- 更多产品
相关分类